
Evoluzione del ruolo delle cellule CHO nello sviluppo di linee cellulari
Dalla prima autorizzazione dell’insulina ricombinante e dell’ormone della crescita umano all’inizio degli anni ’80, una moltitudine di prodotti terapeutici a base di proteine ricombinanti è stata approvata dalle agenzie normative, in particolare l’FDA negli Stati Uniti e l’EMA in Europa. Considerato questo aumento significativo nell’introduzione di successo degli agenti terapeutici biologici, c’è una necessità fondamentale nello spazio della ricerca di nuovi farmaci per supportare processi di produzione più efficienti che richiedono linee cellulari ad alta produttività.
Le cellule ovarie di criceto cinese (CHO) sono una linea cellulare epiteliale altamente suscettibile di trasfezione e sono emerse come standard di riferimento per la produzione di proteine terapeutiche approvate.
Perché vengono utilizzate le cellule CHO?
Diverse proprietà chiave delle cellule CHO hanno guidato la loro affermazione come linea cellulare ospite preferita per le autorizzazioni normative dei prodotti terapeutici ricombinanti:
1
Adattabile alla crescita nella cultura delle sospensione, che è ideale per la produzione su larga scala di bioreattori
2
Adattabile alla crescita in integratori di terreno privi di siero e definiti chimicamente (privi di animali), che garantisce la riproducibilità tra diversi batch di coltura cellulare
3
Consentire modifiche post-traslazionali (ad es. glicosilazioni) alle proteine ricombinanti che sono compatibili e bioattive negli esseri umani
4
Per le cellule CHO sono stati sviluppati diversi sistemi di selezione chimica e amplificazione dei geni, ottimizzati per una resa più elevata di proteine ricombinanti per cellula.
Storia delle cellule CHO
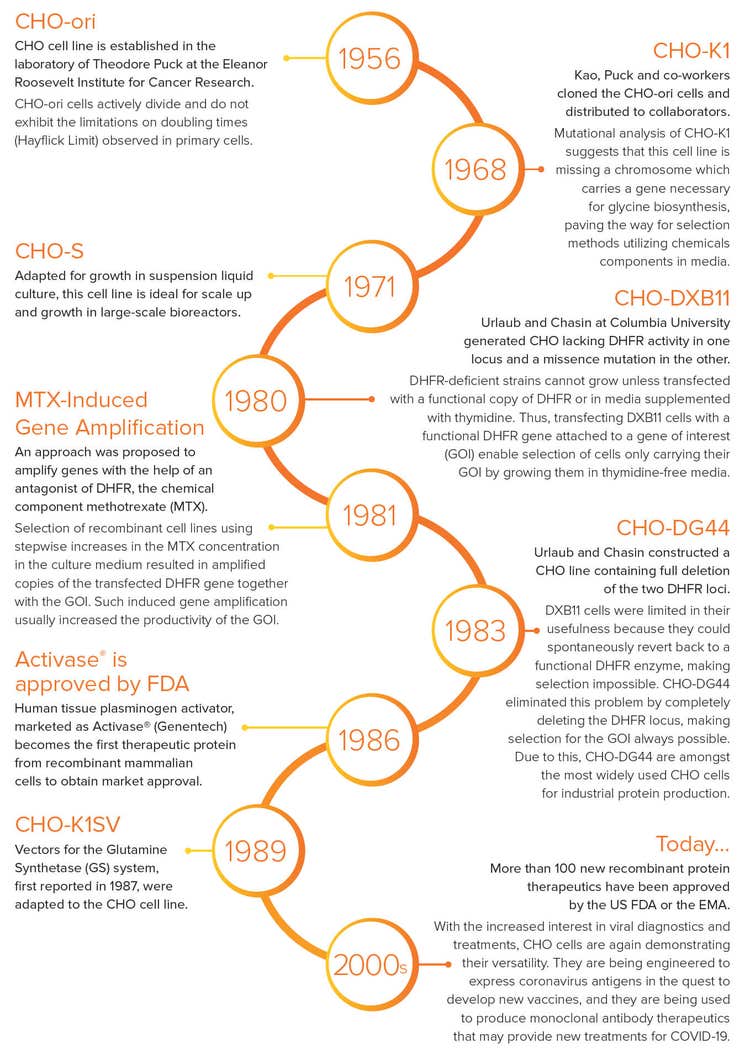
1956 - Cellule CHO-ori
La linea cellulare CHO è stabilita nel laboratorio di Theodore Puck presso l’Eleanor Roosevelt Institute per la ricerca sul cancro. Le cellule CHO-ori si dividono in modo attivo e non presentano le limitazioni sui tempi di raddoppio (limite di sfarfallio) osservati nelle cellule primarie.
1968 - Cellule CHO-K1
Kao, Puck e i colleghi hanno copiato le cellule CHO-ori e distribuito ai dipendenti. L’analisi mutazionale di CHO-K1 suggerisce che a questa linea cellulare manca un cromosoma che trasporta un gene necessario per la biosintesi della glicina, spianando la strada ai metodi di selezione che utilizzano componenti CHO-S delle sostanze chimiche nei supporti.
1971 - Cellule CHO-S
Adattata per la crescita nella coltura liquida in sospensione, questa linea cellulare è ideale per l'incremento e la crescita in bioreattori su larga scala.
1980 - Cellule CHO-DXB11
Urlaub e Chasin alla Columbia University hanno generato CHO senza attività DHFR in un locus e una mutazione di missione nell’altro. I ceppi carenti di DHFR non possono crescere a meno che non siano trasfettati con una copia funzionale di DHFR o in un supporto integrato con timidina. Pertanto, la trasfezione delle cellule DXB11 con un gene DHFR funzionale attaccato a un gene di interesse (GOI) consente la selezione delle cellule che trasportano il loro GOI solo facendole crescere in un supporto privo di timidina.
1981 - Amplificazione del gene indotto da MTX
È stato proposto un approccio per amplificare i geni con l’aiuto di un antagonista del DHFR, il componente chimico metotrexato (MTX). La selezione di linee di cellule ricombinanti utilizzando incrementi a gradini della concentrazione di MTX nel terreno di coltura ha portato a copie amplificate del gene DHFR trasfettato insieme al GOI. Questa amplificazione del gene indotta di solito aumentava la produttività del GOI.
1983 - Cellule CHO-DG44
Urlaub e Chasin hanno costruito una linea CHO contenente la delezione completa dei due loci DHFR. Le cellule DXB11 erano limitate nella loro utilità perché potevano tornare spontaneamente a un enzima DHFR funzionale, rendendo impossibile la selezione. CHO-DG44 ha eliminato questo problema eliminando completamente il locus DHFR, rendendo sempre possibile la selezione per il GOI. Per questo motivo, CHO-DG44 è tra le cellule CHO più utilizzate per la produzione di proteine industriali.
1986 - Activase® è approvato dall’FDA
L’attivatore del plasminogeno del tessuto umano, venduto come Activase® (Genentech) diventa la prima proteina terapeutica dalle cellule di mammifero ricombinanti per ottenere l’approvazione per l’immissione in commercio.
1989 - Cellule CHO-K1SV
I vettori per il sistema di glutamina sintetasi (GS), segnalati per la prima volta nel 1987, sono stati adattati alla linea cellulare CHO.
2000 - Oggi...
Più di 100 nuove terapie proteiche ricombinanti sono state approvato dall’EMA o dalla FDA degli Stati Uniti.
Con l’aumento dell’interesse per la diagnostica e i trattamenti virali, le cellule CHO stanno ancora una volta dimostrando la loro versatilità. Sono stati ingegnerizzati per esprimere gli antigeni del coronavirus nella ricerca di nuovi vaccini e vengono utilizzati per produrre agenti terapeutici a base di anticorpi monoclonali che potrebbero fornire nuovi trattamenti per il COVID-19.
Generare cellule CHO ricombinanti
Scopri un processo efficace e rapido per generare linee cellulari CHO ricombinanti
La selezione di linee di cellule CHO di mammifero ad alta produzione continua a rappresentare un importante collo di bottiglia nello sviluppo del processo per la produzione di prodotti biofarmaceutici. Pertanto, è sempre più importante sviluppare nuovi metodi ad alto rendimento per la selezione di linee cellulari CHO ad alta espressione in modo efficiente ed economico.
In questa nota applicativa, scoprire un processo efficace e rapido per generare linee cellulari CHO ricombinanti, producendo alti livelli di proteine terapeutiche.

I dispositivi Molecolari offrono una soluzione veloce, semplice e completa per lo sviluppo di linee cellulari CHO. Quando combinata con l’agente di rilevazione CloneDetect, l’imager CloneSelect™ e il sistema ClonePix™ , permette ai ricercatori di sviluppare con maggiore efficienza nuove linee cellulari CHO per la produzione di proteine, con conseguente accelerazione dei tempi di commercializzazione.