
Il ruolo di CRISPR nell’ingegneria del microbioma [Podcast]
Il ruolo di CRISPR nelle innovazioni scientifiche nell’ingegneria dei microbi
Le ripetizioni palindromiche brevi regolarmente interspaziate raggruppate (CRISPR) sono state scoperte per la prima volta nel genoma dei batteri marini. Di fronte a una minaccia virale, le cellule batteriche hanno sviluppato una risposta immunitaria catturando e copiando frammenti di DNA di virus. Ciò ha consentito ai batteri di riconoscere gli attacchi successivi e di clivare il DNA virale per arrestare l’infezione virale. È stato anche scoperto che l’enzima Cas era responsabile del clivaggio del DNA. Questo meccanismo di difesa è stato successivamente sfruttato da Doudna e Charpentier, che hanno potuto mirare a una specifica sequenza di DNA e isolarla utilizzando il sistema CRISPR-Cas9 (1).
Nell’ultimo decennio, CRISPR-Cas9 si è dimostrato estremamente prezioso nella scoperta e nella produzione di farmaci. Utilizzando un RNA guida sintetico (gRNA), gli scienziati possono mirare a una sequenza di DNA specifica e utilizzare Cas9 per tagliarla. Successivamente, il macchinario di riparazione dell’ospite cerca di riparare il DNA attraverso un’unione di estremità non omologa (NHEJ), portando a mutazioni casuali che alterano la funzione genica. Utilizzando questo meccanismo, gli scienziati potrebbero ora silenziare i geni per chiarire i loro ruoli nel fenotipo della malattia, il che può portare benefici alla scoperta di target. Inoltre, gli scienziati possono anche utilizzare CRISPR-Cas9 per svelare i meccanismi di farmacoresistenza identificando l’insieme di geni associati all’evasione del sistema immunitario.
Oggi, tuttavia, esploreremo una diversa applicazione di CRISPR: ingegneria del microbioma. A cura di Molecular Devices, il recente episodio del Drug Target Reviews Podcast illustra le applicazioni di CRISPR nell’ingegneria del microbioma e come può superare il collo di bottiglia della ricerca sul microbioma umano.
Unisciti agli esperti leader Dr Jakob Haaber , Vice Presidente e Head of Delivery Technologies, SNIPR Biome e Dr Richard Fox , Co-fondatore, CEO e CTO di Infinome Biosciences, mentre discutono dell'ampia gamma di usi per CRISPR, anche per le terapie e la bioproduzione.
Come CRISPR-Cas9 aiuta a esplorare il ruolo del microbioma umano nelle malattie
Ora è ben noto che il corpo umano contiene trilioni di microrganismi, numerando così le cellule umane. Questi microrganismi, chiamati collettivamente microbioma, formano una simbiosi con l’organismo regolando l’ambiente extracellulare e proteggendo le cellule dai patogeni. Quindi, non sorprende che le alterazioni del microbioma siano strettamente associate a numerose malattie, dal diabete e dall’obesità al cancro.
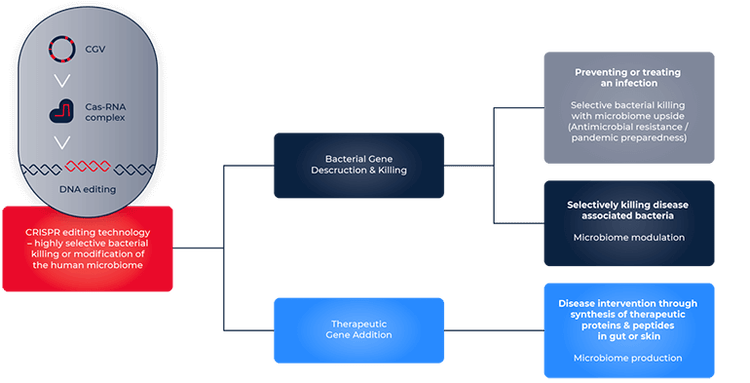
Un modo in cui CRISPR contribuisce alla scoperta farmacologica è la sua implementazione per alleviare le interruzioni del microbioma. Ciò si ottiene progettando sistemi CRISPR-Cas9 per tagliare specifiche sequenze di DNA batterico per eliminare i batteri patogeni. SNIPR Biome è una delle aziende che lavorano attivamente per raggiungere questo obiettivo. Il Dott. Jakob Haaber, Vicepresidente e responsabile di CRISPR e Delivery Technologies presso SNIPR Biome, descrive l’applicazione di CRISPR all’eliminazione patogena di E. coli: “Noi li puntiamo utilizzando il nostro CRISPR che abbiamo programmato per uccidere E.coli. Attualmente, la differenza nella cura per il trattamento delle infezioni batteriche è rappresentata dagli antibiotici. Tuttavia, vi è un aumento dell’insorgenza di resistenza agli antibiotici, che rende gli antibiotici inefficaci. Il vantaggio di CRISPR è che non distingue tra batteri sensibili agli antibiotici e resistenti agli antibiotici. Suggerisce inoltre che CRISPR è in grado di colpire specificamente i batteri patogeni e di risparmiare quelli benefici che sono parte integrante del microbioma intestinale sano, rispetto agli antibiotici con effetti dannosi sui batteri sani insieme ai patogeni.
Vantaggi di CRISPR e dei recenti sviluppi
Secondo Richard Fox, co-fondatore, CEO e CTO di Infinome Biosciences, la forza principale di CRISPR deriva dalla sua capacità di scalare l’editing del genoma. “Invece di mutazioni casuali su un piccolo insieme di geni bersaglio, ora possiamo modificare con precisione un intero percorso o genoma, introducendo centinaia di migliaia di cambiamenti”.
L’editing del genoma su larga scala dà origine a librerie cellulari disponibili in commercio che i ricercatori possono integrare in uno screening fenotipico ad alto rendimento. Queste librerie eliminano la necessità di eliminare manualmente un gran numero di geni per la profilazione fenotipica e propongono una soluzione per l’accelerazione degli studi di scoperta farmacologica.
Un altro vantaggio delle tecnologie CRISPR è la maggiore specificità. L’editing genico del microbioma è uno dei campi che raccolgono i benefici della specificità. I sistemi CRISPR possono essere programmati per tagliare DNA batterico specifico o persino rimuovere circuiti genetici all’interno delle pareti cellulari batteriche senza uccidere la cellula. Nel complesso, questi progressi guidano nuove terapie geniche per le deviazioni microbiote intestinali.
Nel frattempo, i sistemi CRISPR hanno consentito la produzione di costrutti genetici più piccoli per facilitare il confezionamento nei veicoli di consegna. Pertanto, il veicolo di somministrazione può trasportare molteplici componenti oltre a CRISPR, formando una terapia multifunzionale a base genica che realizza molto di più del semplice taglio o inserimento del DNA.
Accelerazione nella produzione di tecnologie CRISPR
Il divario tra biologia sintetica e bioingegneria è spesso causato da problemi relativi a tempi e costi. L'introduzione sul mercato di una soluzione di bioproduzione richiede grandi entità con un'infrastruttura ben costruita, una solida automazione, molte persone, strumentazione, informatica e molto capitale. Quindi, non sorprende che lo sviluppo di farmaci biologici possa richiedere 5-10 anni e molti milioni di dollari. Si tratta di un investimento piuttosto rischioso, quindi le aziende farmaceutiche spesso esitano a parteciparvi, lasciando territori con un enorme potenziale terapeutico inesplorato.
La configurazione del sistema di modifica del genoma abilitato per CRISPR è uno dei colli di bottiglia nei flussi di lavoro. La progettazione di sistemi di ingegneria del genoma su larga scala è piuttosto laboriosa perché potrebbe essere necessario produrre quantità minime di sequenza del donatore per mirare e modificare con precisione i 10.000 loci in un intero genoma.
Uno dei co-fondatori di Infinome Biosciences, Andrew Garst, ha ideato un’innovazione chiave abbinando la sequenza guida che dirige il taglio con la sequenza donatrice che media la riparazione, riducendo così l’editing di un ampio genoma a pochi clic. Richard Fox ritiene che “tali sistemi automatizzati di progettazione e costruzione possano creare librerie di celle modificate in meno di una settimana, che è la frazione dello sforzo che richiedeva”.
Fasi dell’editing genico microbico
Il primo passo nell’editing genico per il microbioma intestinale è la convalida in vitro del sistema CRISPR. La specificità della modifica CRISPR viene testata rispetto a un set di pannelli batterici rappresentativi del microbioma intestinale. Lo scopo è garantire che il sistema CRISPR bersagli una sottospecie predeterminata di batteri e che i batteri benefici siano esenti dall’editing genico indotto da CRISPR
Quindi, la convalida prosegue con gli studi preclinici e clinici. Utilizzando tecniche di sequenziamento del genoma, i ricercatori dimostrano che l’editing genico non perturba il microbioma in modo dannoso. Naturalmente, potrebbero inevitabilmente verificarsi effetti off-target, come rivelato dal sequenziamento dell’intero genoma. La linea d’azione consiste nel monitorare il tasso di occorrenza e garantire che questi effetti siano banali e non interferiscano con l’editing genico.
Il sequenziamento e la profilazione fenotipica rivelano la serie di modifiche trasportate da un genoma, nonché i ceppi prevalenti in una popolazione batterica. Per convalidare ulteriormente il successo dell’editing mirato del genoma, è possibile sottoporre la popolazione batterica a fattori di stress ambientale e monitorarne il comportamento. Ciò garantisce che l’editing genico conferisca ai batteri le proprietà desiderate, ad esempio la capacità di crescere sotto uno stress ambientale come l’ipossia.

Con i flussi di lavoro accelerati di CRISPR, i ricercatori possono ottenere la serie di modifiche geniche benefiche tra centinaia di migliaia di knockout genici.
I sistemi CRISPR sbloccano anche la flessibilità necessaria per arricchire o esaurire lo stesso ceppo batterico a seconda delle specifiche esigenze di ricerca. Ad esempio, i ricercatori di Infinome hanno implementato CRISPR per ingegnerizzare i ceppi di E.coli per aumentare la produzione di lisina, un amminoacido critico utilizzato come additivo alimentare. D’altro canto, SNIPR ha utilizzato lo stesso sistema per eradicare i ceppi nocivi di E.coli dall’intestino dei pazienti con tumore ematologico per prevenire le infezioni del flusso sanguigno.
Guardando al futuro di CRISPR
Come accennato in precedenza, CRISPR potenzia la lotta contro i batteri patogeni. È stato dimostrato diverse volte che i trattamenti antibiotici convenzionali interrompono il microbiota intestinale mirando sia ai batteri dannosi che a quelli benefici. CRISPR può aiutare a migliorare la specificità dei batteri per mantenere l’equilibrio del microbiota intestinale umano.
Un’altra entusiasmante prospettiva guidata da CRISPR è la capacità di ingegnerizzare ceppi batterici con potenziale terapeutico. Questo può essere utilizzato per aggiungere funzioni genetiche al microbioma attraverso batteri ingegnerizzati, che possono esprimere un enzima o un metabolita specifico che l’organismo precedentemente non aveva.
Infine, la riuscita implementazione di CRISPR nell’ingegneria biomedica e bioindustriale si basa sulla capacità di apportare modifiche combinatorie, note anche come “shuffling del DNA”. Soprattutto nei grandi sistemi microbici, la capacità di introdurre più modifiche per ridurre il numero di cicli di screening sarà fondamentale per implementare la produzione bioindustriale.
Molecular Devices aiuta gli scienziati fornendo tecnologie all’avanguardia che accelerano l’obiettivo immediato dell’editing del genoma CRISPR-Cas9. Uno screening accurato della libreria e la selezione dei risultati modificati da CRISPR sono fondamentali nei flussi di lavoro di ingegneria del microbioma, consentendo una più rapida disponibilità del prodotto di bioproduzione sul mercato.
- Doudna, Jennifer A. ed Emmanuelle Charpentier. “La nuova frontiera dell’ingegneria del genoma con CRISPR-Cas9”. Scienza 346,6213 ( 2014): 1258096.
CRISPR在微生物组工程科学突破中的作用
CRISPR首次在海洋细菌的基因组中发现,当面临病毒威胁时,细菌细胞通过捕获和复制病毒的DNA片段来产生免疫反应,这使得细菌能够识别随后的攻击并切割病毒DNA以阻止病毒感染。另外,还发现Cas酶负责切割DNA,这种防御机制后来被Doudna和Charpentier利用,他们可以靶向目标DNA序列,并使用CRISPR-Cas9系统将其分离(1)。
在过去的十年中,CRISPR-Cas9已被证明在药物发现和药物制造中具有巨大的价值。使用合成向导RNA(gRNA),科学家可以靶向目标DNA序列并使用Cas9进行切割。随后,宿主修复机制试图通过非同源末端连接(NHEJ)修复DNA,导致改变基因功能的随机突变。利用这种机制,科学家们现在可以使基因沉默来阐明它们在疾病表型中的作用,这有利于发现目标。此外,科学家还可以利用CRISPR-Cas9,通过识别与免疫系统逃避相关的一组基因来揭示耐药机制。
然而,今天,我们将探索CRISPR的不同应用:微生物组工程。本期内容我们来讨论CRISPR在微生物组工程中的应用以及它如何克服人类微生物组研究的瓶颈。
本次嘉宾:Jakob Haaber博士,副总裁兼交付技术主管SNIPR Biome和Infinome Biosciences联合创始人、CEO 兼CTO Richard Fox博士一起探讨CRISPR的广泛用途,包括治疗和生物制造。
CRISPR-Cas9如何帮助探索人类微生物组在疾病中的作用
众所周知,人体含有数万亿种微生物,在数量上超过了人体细胞。这些微生物统称为微生物组,通过调节细胞外环境和保护细胞免受病原体侵害,与人体形成共生关系。因此,从糖尿病、肥胖到癌症,微生物组的破坏与许多疾病密切相关也就不足为奇了。

通过设计CRISPR-Cas9系统来切割特定的细菌DNA序列以消除致病细菌,这种特异性使CRISPR技术减轻对整体微生物组的破坏,实现药物发现进程的加速。。SNIPR Biome是积极致力于实现这一目标的公司之一,SNIPR Biome副总裁兼CRISPR负责人和交付技术主管Jakob Haaber博士描述了CRISPR在致病性大肠杆菌消除中的应用:“我们使用CRISPR杀死大肠杆菌。目前,治疗细菌感染最常用的就是抗生素。但抗生素耐药性的发生率增加,进而使抗生素无效。CRISPR的优点是它不区分抗生素敏感和抗生素耐药细菌。他还建议,CRISPR可以专门针对致病细菌,而不影响健康肠道微生物组中不可或缺的有益细菌,而不是像抗生素一样,对健康细菌和病原体都有影响。
CRISPR的优势和近年发展

Infinome Biosciences的联合创始人、CEO兼CTO Richard Fox表示,CRISPR的主要优势在于其扩大基因组编辑的能力。“我们现在可以精确地编辑整个通路或基因组,而不是一小部分目标基因上的随机突变,从而引入数十万个变化。
大规模的基因组编辑产生可商用的细胞库,研究人员可以将其整合到高通量表型筛选中。这些库消除了手动敲除大量基因进行表型分析的需要,并为加速药物发现研究提出了解决方案。
CRISPR技术的另一个优点是提高了特异性,微生物组基因编辑是受益于特异性的领域之一。CRISPR系统可以被编程为切割特定的细菌DNA,甚至在不杀死细胞的情况下去除细菌细胞壁内的基因回路。综上所述,这些进步推动了肠道微生物群偏差的新基因疗法。
与此同时,CRISPR系统已经能够制造出更小的基因构建体,以便更容易地装配到递送载体中。因此,除了CRISPR之外,递送载体还可以携带多种成分,构成一种多功能的基于基因的疗法,不仅仅是切割或插入DNA。
加速CRISPR技术的制造
合成生物学和生物工程之间的差距通常是由时间和成本问题引起的。将生物制造解决方案推向市场需要大型实体,这些实体具有完善的基础设施、强大的自动化、大量的人员、仪器、信息学和大量资金。因此,生物制剂的开发可能需要5-10年和数百万美元也就不足为奇了。这是一项风险相当大的投资,因此制药公司往往不愿参与其中,从而一些具有巨大治疗潜力的领域未得到开发。
支持CRISPR的基因组编辑系统的设置是工作流程的瓶颈之一。大规模基因组工程系统的设计非常费力,因为需要产生微量的供体序列来靶向并精确地将10,000个位点编辑到整个基因组。
Infinome Biosciences的联合创始人之一Andrew Garst提出了一项关键创新,将指导切割的引导序列与介导修复的供体序列配对,从而将广基因组编辑减少到只需点击几下。Richard Fox认为,“这种自动化设计和构建系统可以在不到一周的时间内创建编辑过的细胞库,这是过去所花费的努力的一小部分”。
微生物基因编辑步骤
肠道微生物组基因编辑的第一步是CRISPR系统的体外验证。CRISPR编辑的特异性是针对一组代表肠道微生物组的细菌进行测试的,以确保CRISPR系统针对预定的细菌亚种,并且使得有益细菌不受CRISPR诱导的基因编辑的影响。
然后,验证继续进行到临床前和临床研究。利用基因组测序技术,研究人员证明基因编辑不会以有害的方式扰乱微生物组。当然,脱靶效应不可避免地会发生,正如全基因组测序所揭示的那样。我们需要做是监测发生率,并确保这些影响是微不足道的,不会干扰基因编辑。
测序和表型分析揭示了基因组携带的一组编辑以及细菌种群中的主要菌株。为了进一步验证靶向基因组编辑的成功,可以将细菌种群置于环境压力源中并监测其行为。这确保了基因编辑赋予细菌所需的特性,例如在缺氧等环境压力下生长的能力。

通过加速的CRISPR工作流程,研究人员可以在数十万个基因敲除中得到一组有益的基因编辑。
CRISPR系统还可以根据特定的研究需求,灵活地富集或消耗相同的细菌菌株。例如,Infinome的研究人员应用CRISPR来设计大肠杆菌菌株,以扩大赖氨酸的生产,赖氨酸是一种用作食品添加剂的关键氨基酸。另一方面,SNIPR使用相同的系统从血液癌患者的肠道中根除有害的大肠杆菌菌株,以防止血液感染。
展望
如前所述,CRISPR能够对抗致病菌,已多次证明,传统的抗生素治疗通过作用有害和有益细菌来破坏肠道微生物群。CRISPR可以帮助增强细菌的特异性,以维持人类肠道微生物群的平衡。
另一个令人兴奋的前景是设计具有治疗潜力的细菌菌株的能力。这可用于通过工程细菌为微生物组添加遗传功能,这些细菌可以表达身体以前缺乏的特定酶或代谢物。
最后,CRISPR在生物医学和生物工业工程中的成功应用依赖于进行组合编辑的能力,也称为“DNA洗牌”。特别是在大型微生物系统中,引入多次编辑以减少筛选轮次的能力对于生物工业生产至关重要。
Molecular Devices通过提供前沿技术来帮助科学家加速CRISPR-Cas9基因组编辑的近期目标。准确的文库筛选和CRISPR编辑命中物的选择是微生物组工程工作流程的关键,使生物制造产品更快地推向市场。
1. Doudna, Jennifer A.和Emmanuelle Charpentier。“CRISPR-Cas9基因组工程的新前沿。科学346,6213(2014):1258096。