
[Podcast] Difficoltà associate allo sviluppo tradizionale di linee cellulari e tecnologie emergenti che aiutano a controllare la monoclonalità
I progressi compiuti nel campo dell’ingegneria genetica e della biologia sintetica hanno consentito numerosi passi avanti negli ultimi decenni. L’importanza dello sviluppo di linee cellulari richiede una menzione speciale.… Senza di esso, molti vaccini salvavita per malattie infettive, farmaci anticorpali e prodotti proteici ricombinanti, compresa l’insulina, non sarebbero ampiamente disponibili. La fase più impegnativa dello sviluppo di linee cellulari conformi è la garanzia di monoclonalità, principalmente se eseguita manualmente. La monoclonalità delle linee cellulari terapeutiche deve essere realizzata e documentata per motivi normativi.
Nel nostro podcast, “Sviluppo di linee cellulari con la Dott.ssa Natasa Skoko, ICGEB e il Dott. Hugh Graham, MacroGenics”, parliamo dei flussi di lavoro tradizionali per lo sviluppo di linee cellulari e delle tecnologie emergenti per aiutare a verificare la monoclonalità.
Qui abbiamo riassunto i principali punti di discussione dei relatori esperti: Dott.ssa Natasa Skoko, Group Leader dell’Unità di Sviluppo Biotecnologico presso l’International Centre for Genetic Engineering and Biotechnology (ICGEB), e Dott. Hugh Graham, Direttore di Cell Culture Sciences presso MacroGenics.
Sviluppo di linee cellulari
Garanzia di monoclonalità
Tecnologie emergenti e impatto normativo
Significato delle linee cellulari stabili
Nella forma più semplice, il termine linea cellulare definisce una popolazione di cellule che può essere mantenuta in una coltura per un determinato periodo e mantenere un fenotipo, una funzione e una stabilità distinti.
Il Dott. Skoko riassume il significato storico della linea cellulare stabile. “L’uso della linea cellulare ha fatto la rivoluzione, non solo nella ricerca scientifica e ha contribuito a comprendere molti processi biologici fondamentali”, Le sue applicazioni vanno dalla produzione di anticorpi e proteine terapeutiche allo screening farmacologico.
Lo sviluppo di linee cellulari coinvolge cellule di mammifero ingegnerizzate che sono robuste, convenienti e facili da coltivare. Una linea cellulare che soddisfa tutti i criteri è la cellula dell’ovaio di criceto cinese (CHO), sviluppata per la prima volta nel 1987. Oggi, il 70% dei bioterapeutici sul mercato è prodotto da linee cellulari CHO. Sono particolarmente efficienti nella produzione di massa di bioterapeutici, grazie alla loro adattabilità a vari mezzi di crescita e condizioni di crescita (per esempio sospensione, crescita attaccata, lotto alimentato, perfusione), nonché alla loro capacità di piegare e glicosilare le proteine per imitare le modifiche post-traduzionali nelle proteine umane.
Sfide di un flusso di lavoro di sviluppo di linee cellulari tradizionale
La produzione di alti livelli di bioterapeutici si basa sulla generazione di linee cellulari stabili.
La prima fase è la trasfezione di una linea cellulare ospite idonea con il gene di interesse, portando a un’integrazione casuale del DNA nel genoma ospite. Una volta che la linea cellulare ingegnerizzata inizia a crescere, solitamente sotto pressione di selezione, è necessario l’isolamento di una singola cellula per generare cloni per lo screening.
Nei flussi di lavoro tradizionali, le cellule vengono placcate su una piastra 96a pozzetti attraverso la diluizione limitante. Questo metodo prevede la diluizione della sospensione cellulare in modo tale che, quando si placca una certa quantità in un pozzetto, la probabilità che abbia una sola cellula sia molto elevata. Alcuni pozzetti possono anche essere vuoti e alcuni possono avere più cellule. Pertanto, è altamente probabile che una linea cellulare proveniente da uno qualsiasi di questi pozzetti sia sviluppata da una singola cellula.
È fantastico, ma quanto tempo ci vuole? Ipotizzando che le cellule raddoppino in numeri ogni 24 ore, sono necessari dieci raddoppi per raggiungere mille cellule, il che richiederebbe 10 giorni. Per ottenere una quantità di cellule sufficiente con cui lavorare, sarebbero necessarie 2-3 settimane. Inoltre, le normative sulla monoclonalità richiedono di ripetere la diluizione limitante per avere un’ulteriore garanzia dell’origine clonale della linea cellulare. Quindi, dovresti trascorrere mesi per ottenere risultati da questo metodo a basso rendimento. Il Dott. Graham aggiunge: “La stabilità della linea cellulare viene messa alla prova. Quando raggiungi i numeri auspicabili e hai un’elevata garanzia di monoclonalità, c’è la possibilità che si siano spostati nelle loro proprietà, abbiano perso alcune copie del gene di interesse o si siano adattati in un modo che non ti aspettavi”.
Per riassumere, limitare la diluizione può non riuscire a raggiungere velocità, conformità e qualità della linea cellulare perché è difficile documentare la monoclonalità e mantenere la qualità delle cellule. Sia il Dott. Skoko che il Dott. Graham concordano sul fatto che l’automazione è il modo per facilitare la crescita della linea cellulare monoclonale ad alto rendimento e la sua documentazione.
Elementi essenziali della linea cellulare monoclonale
Ora facciamo un passo indietro per definire la monoclonalità. Una linea cellulare monoclonale ha origine da una singola cellula o da un singolo progenitore.
Perché è così importante? Quando le cellule iniziano a crescere e raddoppiare, sono soggette a derive genetiche, mutazioni o perdita di un plasmide. Quindi, è quasi impossibile garantire che la qualità delle proteine terapeutiche che esprimono sia uniforme semplicemente studiando il loro fenotipo più recente.
Per compensare ciò, è necessario iniziare a documentare le cellule il Giorno Zero per dimostrare che provenivano effettivamente da una singola cellula.

La crescita cellulare di CHO-s è stata utilizzata per acquisire immagini dalle piastre 6a pozzetti in più punti temporali. Il Giorno 0, si osserva chiaramente nella riga superiore che una cellula è presente mentre nella riga inferiore sono osservate due cellule. Il cerchio giallo mostra la posizione di una bead che funge da riferimento di posizione per confermare che la stessa colonia viene acquisita nel tempo.
Tipica evidenza di monoclonalità che i regolatori cercano è basata sull’immagine, vale a dire che l’immagine di una singola cellula deve essere registrata.
L'apparecchiatura più efficace per lo sviluppo di linee cellulari monoclonali è una stampante a cella singolache esegue la deposizione a cella singola. Altri metodi includono il Fluorescence-Activated Cell Sorting (FACS) e flussi di lavoro che automatizzano ogni fase, dall’incubazione al pipettaggio.
Importanza della verifica della monoclonalità precoce
La garanzia della monoclonalità in una fase iniziale ha diverse implicazioni per le applicazioni nel settore delle scienze biologiche. Il Dott. Graham sottolinea il significato della monoclonalità per il ciclo di sviluppo del farmaco: “Ci sono linee cellulari e molecole in fase di commercializzazione che sono state sviluppate dieci o più anni fa. I processi di clonazione di dieci anni fa potrebbero non disporre della documentazione necessaria per garantire un’origine clonale. Quando si porta una linea cellulare di questo tipo a un regolatore, potrebbe essere chiesto di dimostrare che proviene originariamente da una linea cellulare clonale. Se non hai questa prova, dimostrarla più avanti nel progetto è molto lavoro”.
Il Dott. Skoko aggiunge: “Si tratta di ridurre al minimo i rischi e di avere un processo di produzione e una qualità del prodotto coerenti. Ecco perché è essenziale garantire la monoclonalità fin dalla fase iniziale. Iniziare con una banca di cellule con un’elevata garanzia di monoclonalità comporta meno lavoro in un secondo momento. Inoltre, eviterete gravi interruzioni nella produzione e ridurrete l’incertezza quando apporterete modifiche al processo di produzione”.
Tecnologie monoclonali emergenti per verificare le linee cellulari singole
Le tecniche emergenti per l’imaging e la coltivazione delle linee cellulari monoclonali sono in crescita. Ecco alcuni esempi:
- La sospensione cellulare semi-solida, per cui una singola cellula cresce in una sospensione semi-solida, può essere acquisita man mano che cresce.
- Un anello di clonaggio che circonda una singola cellula per isolarla e proteggerla dalla contaminazione
- FACS: Ordinamento delle cellule in base alle caratteristiche fluorescenti
- Stampanti microfluidiche a celle singole basate su gocce con la possibilità di acquisire immagini di pozzetti appena placcati contenenti celle singole
Questi metodi combinati migliorano la credibilità delle evidenze di monoclonalità.
Naturalmente, esiste un grande potenziale per migliorare le tecniche attuali e inventare tecniche superiori. Innanzitutto, le evidenze visive, ovvero l’imaging a singola cellula, devono essere utilizzate più spesso poiché superano le sfide legate ai costi e ai tempi di limitazione della diluizione e dell’ordinamento della citometria a flusso.
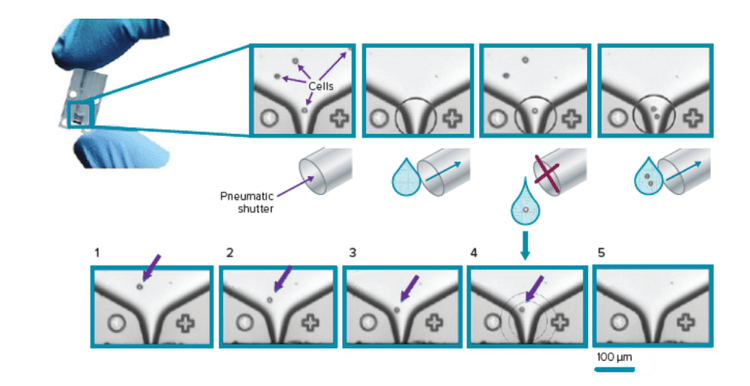
La serie di stampanti a cella singola CloneSelect è un sistema completamente automatizzato che utilizza la tecnologia proprietaria basata sulla microfluidica e l’analisi delle immagini in tempo reale per ordinare e depositare singole cellule in micropiastre standard, garantendo al contempo la monoclonalità attraverso la documentazione delle immagini.
Ulteriori miglioramenti sono possibili lungo la linea di produzione. Ad esempio, migliorare i metodi analitici nella produzione di proteine terapeutiche può aiutarci a monitorare l’intero processo di produzione. Ciò porta la variazione genetica sotto controllo e garantisce l’uniformità della proteina prodotta.
Un’altra preoccupazione nello sviluppo di linee cellulari monoclonali è la velocità. Come sottolinea il dott. Graham, “attendere che una linea cellulare clonale produca la proteina in clinica è una barriera in termini di tempo. Oggi, le persone si stanno spostando verso i primi lotti di proteine da pool di cloni precoci per il primo materiale clinico di buona pratica di fabbricazione (GMP). Quindi, si genera la linea cellulare clonale per le sperimentazioni cliniche in fase avanzata e la produzione GMP. Eliminare la necessità di una prova di origine clonale nelle prime sperimentazioni cliniche è un approccio interessante per accelerare lo sviluppo di bioterapeutici. Tuttavia, questo approccio potrebbe richiedere ulteriore lavoro per ottenere l’approvazione normativa”.
Il ruolo della regolamentazione e il suo impatto sul processo di sviluppo delle linee cellulari
Come potete vedere, le normative influiscono innegabilmente sullo sviluppo di linee cellulari monoclonali. Una implicazione di normative rigorose è che il produttore deve fornire un rapporto completo sulla linea cellulare monoclonale prima di richiedere l’approvazione. Una prova insufficiente o documenti mancanti possono comportare ritardi normativi o ulteriori impegni post-approvazione. Poiché l’approvazione normativa richiede un eccellente supporto scientifico, è meglio fornire il maggior numero di prove possibile sin dalle prime fasi, specialmente per l’origine clonale.
Cosa riserva il futuro ai flussi di lavoro delle linee cellulari monoclonali?
Ci sono sfide irrisolte nei flussi di lavoro delle linee cellulari monoclonali, tra cui preoccupazioni finanziarie, ottenere risultati ad alto rendimento e garanzia dell’origine monoclonale.
Rispetto ai metodi legacy, gli odierni sviluppatori di linee cellulari monoclonali dispongono di strumenti molto migliori per garantire la conformità normativa e la qualità delle linee cellulari.
Una prospettiva entusiasmante è una migliore gestione dei dati, necessaria per organizzare set di dati di grandi dimensioni generati da studi sullo sviluppo di linee cellulari. La combinazione della gestione dei dati con il machine learning può dare origine a una piattaforma che prevede la qualità di un bioterapeutico basata esclusivamente sull’origine clonale.
Il ruolo dell'automazione diventerà anche più fondamentale in termini di velocità e coerenza. Più specificamente, l'automazione può accelerare lo sviluppo di cloni e lo screening delle colonie. Il dott. Skoko chiarisce gli effetti dell'automazione: “Stiamo parlando di screening dei 10.000cloni tra un paio di settimane. Un flusso di lavoro tradizionale richiederebbe da 30 settimane a due anni. La tecnologia automatizzata può aiutarci ad avere cloni accurati, eliminare gli errori associati alla tradizionale diluizione limitante e superare il lavoro con una popolazione eterogenea di diversi secretori. Puoi valutare la stabilità dei tuoi cloni fin dall’inizio”.
Flusso di lavoro automatizzato per lo sviluppo di linee cellulari con garanzia di monoclonalità
Grazie all'integrazione delle tecnologie di automazione, è possibile selezionare centinaia di migliaia di cloni per trovare quel clone dorato in grado di generare il rendimento più elevato per la proteina di vostro interesse. Cosa ancora più importante, ti aiuta a documentare completamente ogni fase del processo di sviluppo a partire dal giorno zero. In ultima analisi, puoi risparmiare tempo e denaro evitando conflitti futuri causati dalla mancanza di garanzia di monoclonalità o dalla qualità incoerente del prodotto.
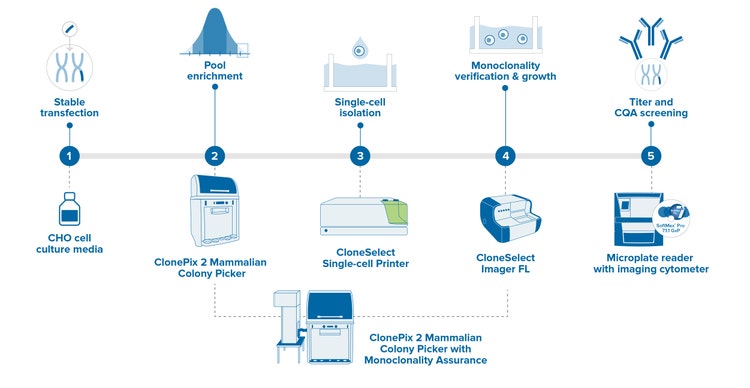
Accelera le tempistiche di sviluppo delle linee cellulari integrando più passaggi in un unico passaggio. Il sistema potenziato ClonePix 2 Mammalian Colony Picker con garanzia di monoclonalità può eseguire automaticamente lo screening e la selezione di cloni sia ad alta produzione che monoclonali, il tutto in un unico sistema. Possibilità di screening di un maggior numero di cloni in meno tempo grazie alla verifica della monoclonalità al giorno zero e a un processo di screening e prelievo dei cloni più produttivi che dura meno di due settimane. La funzione di rapida acquisizione su piani multipli (z-stack) permette la rilevazione di singole cellule nell’intero volume del terreno, e non in un unico piano focale, al giorno

Molecular Devices dispone di un solido portafoglio per automatizzare il flusso di lavoro e le tecnologie di sviluppo delle linee cellulari per garantire la monoclonalità, tra cui il prelievo di cloni, l’isolamento e l’imaging di singole cellule e i lettori per micropiastre. Le nostre collaudate soluzioni GxP aiutano a garantire l’integrità dei dati e la conformità per i laboratori GMP/GLP.
Scopri di più sullo sviluppo di linee cellulari e sulle applicazioni di monoclonalità o parla con uno specialista dell'automazione se sei interessato a esplorare una soluzione automatizzata per il tuo laboratorio.